脑卒中,俗称“中风”,因其高发病率、高致残率和高死亡率,一直是笼罩在人类健康上空的阴霾。其中,缺血性脑卒中(由血管堵塞引起)最为常见,占所有病例的80%以上。即便在及时抢救后,脑血管重新开通(医学上称为“再灌注”)引发的二次损伤也常常让神经功能雪上加霜,导致患者遗留偏瘫、失语等严重后遗症。在这一复杂的损伤过程中,一种名为“铁死亡”的细胞死亡方式,被证实是导致神经元坏死的关键“元凶”之一,也是制约脑卒中疗效的核心难题。

近日,一项发表在国际知名期刊《Advanced Healthcare Materials》上的研究,为攻克这一难题带来了曙光。复旦大学附属闵行医院赵静教授团队首次深入揭示了人脐带间充质干细胞来源的外泌体,是如何精准“狙击”神经元铁死亡,从而保护大脑的。

人脐带间充质干细胞外泌体(hUMSC-Exos),可以理解为干细胞释放的“微型快递包裹”,它们携带着蛋白质、核酸等生物信息,在细胞间传递信号。此前,科学家们已发现这类外泌体对神经有保护作用,但最大的疑问在于:大脑为了安全,设有一道几乎无法逾越的“防火墙”——血脑屏障,外泌体能否顺利进入大脑并发挥作用呢?
团队首先对外泌体进行了严格的制备和鉴定,确认其符合标准。接着,他们通过一种无创的“经鼻给药”方式进行了实验。令人惊喜的是,这些外泌体成功穿越了血脑屏障,并像安装了“导航”一样,精准地聚集在大脑缺血的损伤区域(半暗带),并被神经元所摄取。在小鼠模型中,接受外泌体应用的动物,其脑组织损伤范围明显缩小,神经功能也得到了显著改善。这证实了hUMSC-Exos不仅能到达战场,更能有效地保护神经。
那么,这些外泌体究竟是如何发挥保护作用的呢?研究团队利用先进的分子生物学技术,层层剥茧,最终锁定了一条关键的通路。
他们发现,在脑缺血再灌注后,神经元内一个名为 ARRDC3 的蛋白会异常增多。这个分子就像一个“破坏分子”,它会激活另一个蛋白 DRP1,导致细胞内的“能量工厂”——线粒体发生过度分裂。线粒体本是维持细胞生命活动的核心,一旦分裂失控、碎片化,就会引发级联反应,最终导致神经元发生“铁死亡”。简言之,ARRDC3–DRP1 这条信号轴的异常激活,就是开启神经元死亡的“开关”。
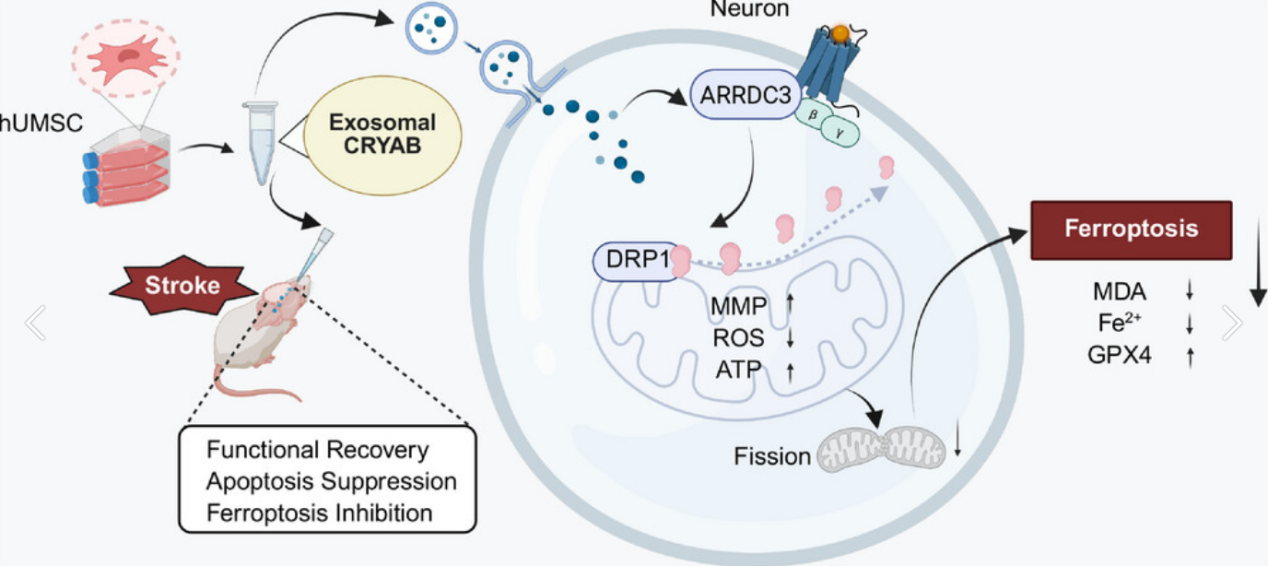
(神经元中hUMSC-Exos介导的功能信号通路示意图。)
而干细胞外泌体的“神奇之处”在于,它内部富含一种叫做 CRYAB 的蛋白质。研究发现,hUMSC-Exos正是通过其携带的CRYAB蛋白,精准地抑制了ARRDC3–DRP1信号轴的异常激活,让线粒体恢复正常的融合与分裂平衡(即维持线粒体动力学稳态),从而从源头上阻断了铁死亡的发生。
为了验证CRYAB的核心地位,团队使用了一种抑制剂来阻断CRYAB的功能。结果发现,当CRYAB被抑制后,外泌体对神经元的保护作用几乎消失,线粒体再次出现碎片化,铁死亡相关的指标也显著升高。这直接证明了,CRYAB是外泌体发挥神经保护作用的“核心蛋白”。
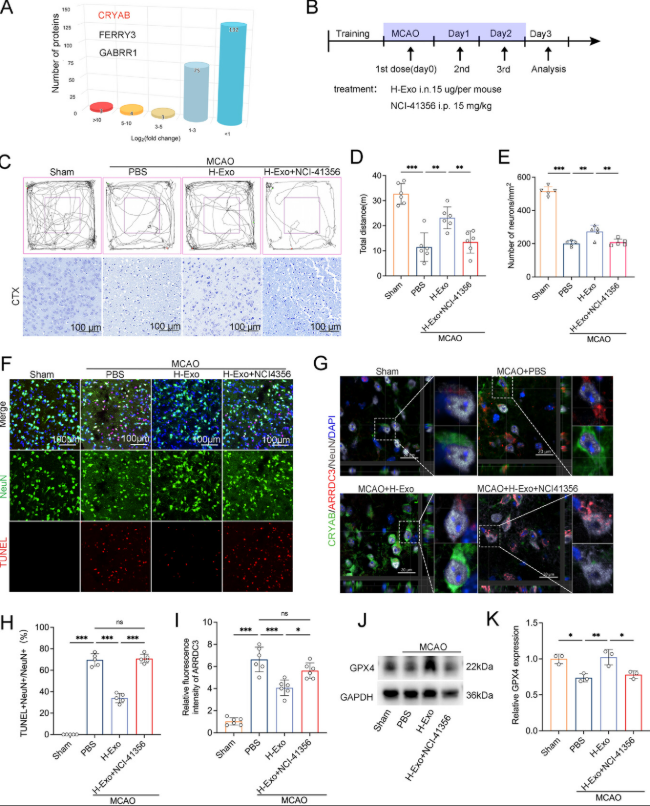
(hUMSC-Exos通过CRYAB介导的ARRDC3抑制作用促进神经保护和功能恢复。)
这项研究的意义在于,它第一次系统地阐明了脐带间充质干细胞外泌体是通过 CRYAB–ARRDC3–DRP1 这条全新的分子通路,来调控线粒体稳态、抑制神经元铁死亡的。
这一发现不仅深化了我们对脑卒中后神经损伤机制的理解,更重要的是,它为临床治疗指明了新方向:
提供新靶点:CRYAB、ARRDC3、DRP1 这些关键分子,未来都可能成为研发精准治疗药物的新靶点。
优化给药方式:研究采用的“经鼻给药”方式,操作简便、无创且能高效递送药物至大脑,为外泌体的临床应用铺平了道路。
脑卒中的治疗是漫长的科学攻坚之旅。复旦大学这项研究成果,为干细胞疗法在神经系统疾病中的应用提供了坚实的理论依据,随着研究的深入,这项成果有望转化为切实有效的治疗方案,为全球数千万脑卒中患者及其家庭带来康复的新希望。
https://pubmed.ncbi.nlm.nih.gov/41555725/
https://mp.weixin.qq.com/s/MVkYmmI9CiyCUlz5pm69Ng