转自:医学界
HER2作为重要的肿瘤生物标志物,其异常表达可见于多种实体瘤,不仅限于传统认知中的乳腺癌和胃癌。近年来,HER2检测在更多瘤种中的临床意义日益受到关注,相关靶向药物的研发也拓展了HER2异常的临床应用前景。然而,在真实世界诊疗环境中,不同肿瘤类型中HER2免疫组化(IHC)高表达(IHC3+)的分布特征与流行病学数据仍不明确,这限制了我们对HER2阳性肿瘤整体疾病负担的理解,也影响了精准检测路径在临床实践中的系统化推进。
近日,JAMAOncology在线发表了一项大规模真实世界研究的简报,分析了超过65,000例实体瘤患者的HER2IHC检测数据,系统揭示了HER2IHC3+在不同瘤种中的阳性率及分布情况[1]。该研究为理解HER2在泛瘤种中的表达谱提供了重要流行病学参考,也为未来优化生物标志物检测策略、推动精准诊疗实践带来启示。此类大规模真实世界证据也有助于识别可能从后续更精细分子分型中获益的瘤种,为构建更高效的临床检测路径奠定基础。本文对该研究的主要内容进行梳理和概述,以期为相关领域临床工作者提供参考。
研究方法
本研究为一项回顾性观察性研究,分析了2024年6月1日至12月31日期间接受HER2免疫组化检测的65,075例患者样本。数据分析涵盖了肿瘤类型、HER2IHC评分和标本类型(活检或切除标本)。对于非乳腺癌病例,HER2IHC3+的判读根据胃腺癌的活检或切除标准进行(取决于标本类型)[2];对于乳腺癌病例,则遵循美国临床肿瘤学会/美国病理学家协会(ASCO/CAP)的乳腺癌指南进行评分。本研究未纳入HER2IHC2+且原位杂交(ISH)阳性的病例。所有HER2状态均由具有资质的病理医师进行判读。
研究结果
本研究在超过65,000例实体瘤中评估了HER2IHC3+的阳性率。如表1所示,总体泛肿瘤阳性率为3.1%(2,032/65,075),但不同肿瘤类型间的差异显著。阳性率最高的肿瘤类型为膀胱癌(13.9%)和子宫浆液性癌(13.6%),而神经胶质瘤、肉瘤等多种肿瘤中则未发现任何HER2IHC3+病例。
此外,研究还比较了在非乳腺癌肿瘤中,采用胃腺癌活检标本与切除标本判读标准进行判读的结果。数据显示,在阳性率≥0.4%的非乳腺肿瘤中,对于大多数肿瘤类型,基于活检标本与基于切除标本得出的HER2IHC3+阳性率基本相似(图1)。
表1.不同肿瘤类型的HER2IHC3+阳性率(2024年6-12月)
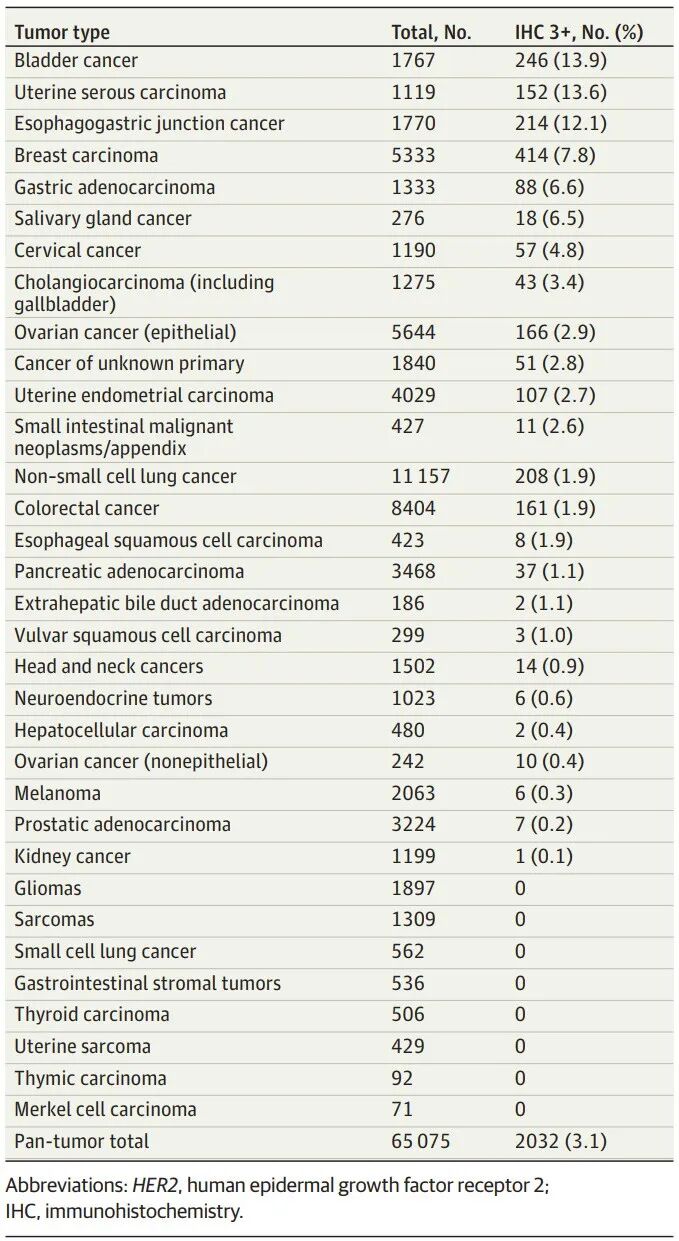
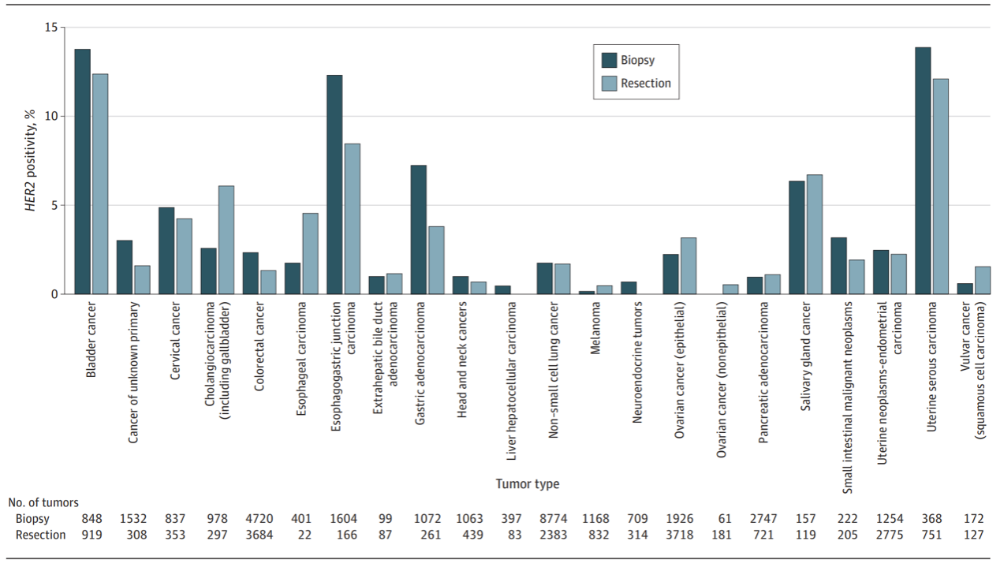
图1基于活检与切除标本判读标准的HER2阳性率(IHC3+)比较(按肿瘤类型)
总结
本研究首次在大规模真实世界队列中,系统性地描绘了HER2IHC3+在泛瘤种中的分布图谱。核心发现是HER2强阳性在不同肿瘤类型中分布极不均衡,总体阳性率为3.1%,其中膀胱癌、子宫浆液性癌和食管胃结合部癌的阳性率最高(>12%),而神经胶质瘤、肉瘤等多种肿瘤中未发现阳性病例,前列腺癌、肾癌等瘤种的阳性率也极低。
这些发现对临床实践具有重要启示:在当前背景下,对所有实体瘤进行无差别的、普适性的HER2IHC检测可能并非必要,尤其是在那些阳性率极低或为零的肿瘤类型中。从医疗必要性和成本效益角度出发,本研究为优化检测策略提供了关键证据。值得注意的是,除乳腺癌外,本研究中其他瘤种均采用胃癌的HER2检测和判读标准。在胃癌中,活检标本通过强HER2染色肿瘤细胞的数量进行评估,而切除标本则通过强染色肿瘤细胞的百分比进行评估。研究数据显示,各肿瘤类型中活检与切除标本的阳性率相近,这支持了这些胃癌中针对活检与切除标本的不同判读标准可推广至其他瘤种,这为检测标准化提供了依据。
研究者进一步提出,或可考虑采用综合基因组分析作为筛查工具,优先对存在ERBB2基因扩增和/或ERBB2信使RNA过表达的肿瘤进行HER2IHC验证,这种分流策略有助于优化实验室工作流程,减少不必要的检测,从而更精准、高效地识别出可能从抗HER2治疗中获益的HER2阳性晚期实体瘤患者。当然,研究也存在一定局限性,其数据来源于商业实验室,患者群体可能与常规医疗机构有所不同,在结果外推时需保持谨慎。
参考文献:
[1]BryantD,FeldmanR,AbdullaF,etal.AReal-WorldExperienceinPan-TumorTestingforHER2IHCinMoreThan65000SolidTumors.JAMAOncol.PublishedonlineJune26,2025.
[2]BartleyAN,WashingtonMK,ColasaccoC,etal.HER2TestingandClinicalDecisionMakinginGastroesophagealAdenocarcinoma:GuidelineFromtheCollegeofAmericanPathologists,AmericanSocietyforClinicalPathology,andtheAmericanSocietyofClinicalOncology.JClinOncol.2017;35(4):446-464.
审批编号:CN-171663有效期至:2026-11-19
本材料由阿斯利康提供,仅供医疗卫生专业人士参考