在肿瘤治疗领域,放射治疗是常用的手段之一,但放射性皮肤损伤这一并发症却让不少患者和医生头疼不已。据相关数据表明,在接受放疗的患者中,有85%至95%都会出现不同程度的皮肤反应。一开始可能只是皮肤出现红斑、脱屑等轻微症状,然而随着病情发展,极有可能演变成经久不愈的慢性溃疡。这不仅严重影响了肿瘤治疗的连贯性,让治疗进程受阻,更极大地降低了患者的生活质量,给患者带来诸多痛苦和不便。
但令人无奈的是,目前临床上针对这类放射性皮肤损伤,还没有一套统一且特效的治疗方案。医生们大多只能依靠经验进行对症处理,这就使得开发更有效的治疗手段变得尤为迫切,成为医学界亟待攻克的难题。
不过,最近医学领域有了新发现,外泌体或许能成为解决这一难题的“救星”。外泌体是细胞释放出来的一种纳米级囊泡,别看它个头小,作用可不小。它就像一个“信息快递员”,携带了蛋白质、核酸等信号分子,能够在细胞之间传递信息,介导细胞间的通讯。而且,外泌体作为一种“无细胞治疗”制剂,有着独特的优势。它不仅保留了干细胞的修复能力,还具备安全性高、易于保存和运输、免疫排斥风险低等特点,这让它成为了医学研究的热点。

齐齐哈尔医学院的研究团队就在外泌体研究方面取得了重要进展。他们在《科学报告》期刊上发表了一项研究,系统评估了骨髓间充质干细胞来源的外泌体对大鼠放射性皮肤损伤的治疗效果,还深入探究了其背后的作用机制。
在实验过程中,研究人员先成功分离并提取出了骨髓间充质干细胞外泌体。接着,他们构建了大鼠放射性皮肤损伤模型,并把实验动物分成了三组:对照组、单纯辐射组以及外泌体治疗组(在大鼠皮肤损伤局部注射干细胞外泌体)。经过21天的仔细观察,结果令人惊喜。和未接受治疗的组相比,接受外泌体治疗的大鼠,皮肤损伤面积明显缩小,愈合速度也大大加快。
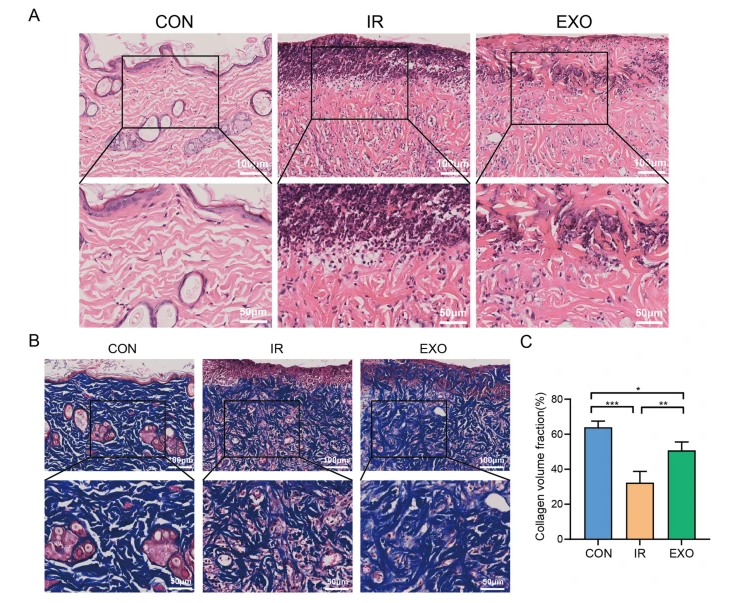
(插入图片:BMSCs - Exos对放射性皮肤损伤(RISI)的影响及组织学分析)进一步的病理学分析,为我们揭开了外泌体促进皮肤修复的几个关键秘密。首先,外泌体能够改善创面的组织结构,促进表皮再生,还能让胶原蛋白有序沉积,把原本紊乱的胶原纤维排列修复得整整齐齐。其次,外泌体具有促进血管生成的作用。它能提升损伤部位血管内皮标志物和血管平滑肌标志物的表达。这意味着什么呢?简单来说,就是新生的毛细血管增多了,而且血管结构变得更加成熟稳定,这样就能为正在修复的组织提供充足的血液和营养供应,让修复工作进行得更加顺利。
那外泌体究竟是通过什么具体机制来发挥作用的呢?研究团队把重点放在了“炎症调节”和“细胞凋亡”这两个核心环节上。
放射性损伤往往会伴随着持续的过度炎症反应,这就像给组织修复工作设置了一道“障碍”,严重阻碍了组织的愈合。研究发现,外泌体能够调节局部免疫环境,诱导巨噬细胞向具有抗炎作用的M2表型转化。这一转化直接带来了积极的效果,促炎因子(如TNF - α、IL - 1β)减少了,抗炎因子(如IL - 10)增加了,从而有效地控制了损伤部位的炎症状态,为组织修复创造了良好的环境。
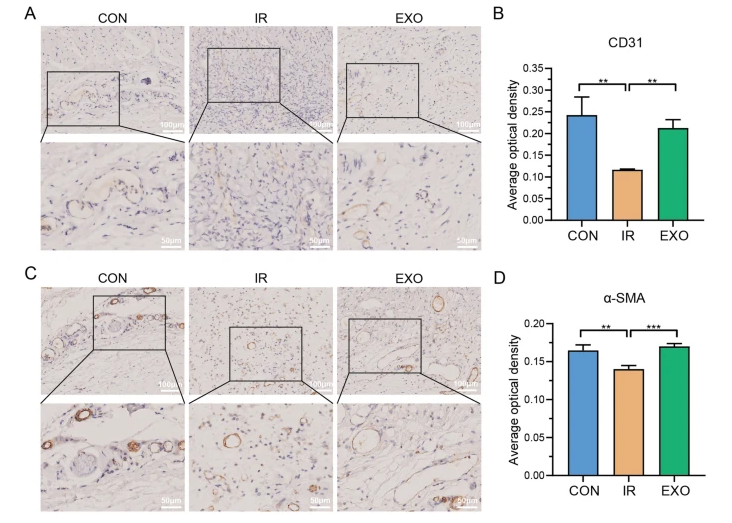
(插入图片:BMSCs - Exos对放射性损伤皮肤组织(RISI)血管生成的影响)同时,辐射还会导致大量皮肤细胞凋亡,这无疑会影响组织的再生能力。但在外泌体处理组的大鼠中,损伤部位凋亡细胞数量明显减少。从分子层面来看,外泌体上调了抗凋亡蛋白Bcl - 2的表达,下调了促凋亡蛋白Bax,还激活了与细胞存活密切相关的Akt信号通路。体外实验也证实,这些外泌体能够被人体皮肤成纤维细胞摄取,并且显著促进其迁移能力,而细胞的迁移能力对于创面愈合可是至关重要的。
这项研究具有重大的意义,它首次系统证实了骨髓间充质干细胞外泌体对放射性皮肤损伤的治疗价值,明确了外泌体通过“抗炎”和“抗凋亡”双管齐下,协同促进组织修复的核心机制。这一发现为放射性皮肤损伤这一临床难题提供了有前景的治疗新策略。未来,随着研究的不断深入,这种基于外泌体的疗法有望为更多难愈性创面的修复提供重要的参考思路,给广大患者带来新的希望。让我们共同期待外泌体在医学领域创造更多的奇迹!