当60岁的詹妮弗·罗伯逊(Jennifer Robertson)在2024年成为欧洲首位接受个性化mRNA癌症疫苗治疗的患者时,她可能没有想到,自己正站在一场医学革命的最前沿。这位来自苏格兰邓迪的胃食管癌患者,在接受手术和化疗后,又接受了一种名为mRNA-4157(V940)的个体化新抗原疗法。这种疗法与新冠疫情期间广泛使用的mRNA疫苗采用相似技术,但目标更为精准,教会她自身的免疫系统识别并攻击癌细胞。
如今,她已经摆脱了癌症的困扰,并为自己能推动医学进步而感到自豪。

图片来源于Universityof Dundee
詹妮弗的故事并非孤例。在全球范围内,癌症疫苗正从实验室走向临床,从概念变为现实。这背后,是一场深刻改变癌症治疗格局的科学革命。
传统癌症治疗如手术、化疗和放疗,往往伴随着巨大的身心创伤和难以避免的副作用。更重要的是,它们难以彻底清除所有癌细胞,导致复发风险居高不下。而免疫治疗,特别是癌症疫苗,代表了一种全新的“精准制导”思路。
癌症疫苗训练患者的免疫系统识别癌细胞表面的特定标志物(新抗原)。这些新抗原是癌细胞因基因突变而产生的独特蛋白质片段,正常细胞中不存在。通过向免疫系统展示这些“通缉令”,癌症疫苗能够激活T细胞等免疫细胞,使其像训练有素的“特种部队”一样,精准定位并清除癌细胞。

新冠疫情意外加速了mRNA技术在医学领域的应用。mRNA疫苗的快速研发和大规模生产证明了这项技术的可行性和安全性,为癌症疫苗的发展铺平了道路。
mRNA-4157疫苗在黑色素瘤治疗中取得突破
与传统疫苗相比,mRNA疫苗具有研发周期短、易于规模化生产、安全性较高等优势。Moderna的mRNA-4157疫苗,在针对高风险黑色素瘤的临床试验中已显示出令人鼓舞的结果:与Keytruda联合使用,可将复发或死亡风险降低49%。
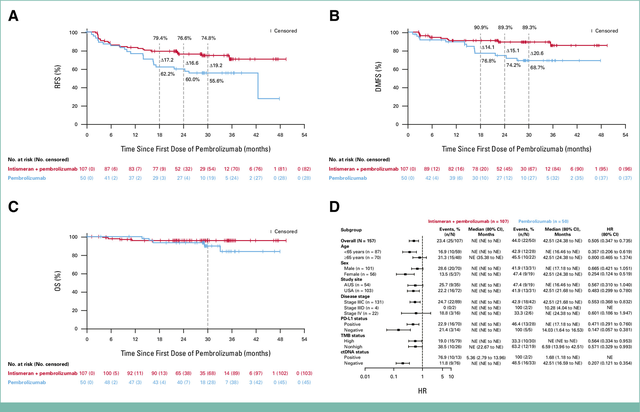
近日,《JCO Oncology Advances》发表的mRNA-4157联合帕博利珠单抗对比帕博利珠单抗辅助治疗已切除黑色素瘤的随机IIb期研究三年更新数据显示:
联合治疗方案对比单独使用帕博利珠单抗辅助治疗已切除黑色素瘤的疗效结果令人振奋:
无复发生存率(RFS):1.5年时,联合治疗组79.4%,单药组62.2%;2年时,联合治疗组76.6%,单药组60%;2.5年时,联合治疗组74.8%,单药组55.6%;
远处无转移生存率(DMFS):1.5年时,联合治疗组90.9%,单药组76.8%;2年时,联合治疗组89.3%,单药组74.2%;2.5年时,联合治疗组89.3%,单药组68.7%。
全球研发浪潮:癌症疫苗在多种癌症中展现潜力
詹妮弗参与的mRNA-4157疫苗试验,只是全球癌症疫苗研发浪潮中的一朵浪花。目前,全球已有数十种治疗性癌症疫苗进入临床研发阶段,覆盖了肺癌、肝癌、胰腺癌、黑色素瘤、胃癌等主要癌种。
肾细胞癌
一项I期试验显示,9名晚期透明细胞肾细胞癌患者接受个性化肽疫苗后,中位随访40.2个月无一人复发。
非小细胞肺癌
古巴CIMAvax-EGF疫苗通过激活免疫系统,促使人体产生抗体,从而阻止表皮生长因子与癌细胞结合。癌细胞便无法获得其赖以生存的蛋白质,最终走向死亡。
临床数据显示,在晚期非小细胞肺癌患者中,中位总生存期(OS)为22.46个月,半年的总生存率高达97.7%,1年生存率为82.7%。
头颈癌
1月21日,德国BioNTech公司的mRNA癌症疫苗BNT113也因其在HPV16阳性头颈癌中的潜力获得了FDA的快速通道资格,有望加快研发进程。
2024年欧洲肿瘤内科学会(ESMO)上报告了BNT113+帕博利珠单抗在HPV阳性头颈部鳞状细胞癌(HNSCC)中的试验结果,中位总生存期(OS)达到22.6个月。
中国力量:本土创新不容小觑
在国际巨头领跑的同时,中国的科研团队也在这一领域取得了显著进展:
立康生命科技自主研发的肿瘤新生抗原mRNA疫苗产品LK101注射液联合常规消融治疗在肝细胞癌(HCC)患者中的研究(NCT03674073)结果显示:LK101治疗组有18.2%的患者在1年内复发,低于对照组33.3%的患者复发率,LK101治疗组36.4%的患者在2年时间内复发,同样低于对照组51.4%的患者复发率。由此可见,LK101的联合治疗方式可有效降低患者的复发率。
尽管前景广阔,但我们必须清醒地认识到,绝大多数癌症疫苗仍处于临床试验阶段,尚未成为标准治疗方案。
结语
从mRNA-4157在黑色素瘤中展现的显著疗效,到全球数十种癌症疫苗在肺癌、肝癌、胃癌等领域的积极探索,再到中国本土创新如LK101疫苗在肝细胞癌治疗中取得的进展,癌症疫苗的研发浪潮正以前所未有的速度推进。尽管绝大多数疗法仍处于临床试验阶段,尚未成为标准治疗,但科学界已清晰看到其变革潜力。詹妮弗的故事只是一个开始,而这场关乎生命的革命,正在全球科研人员与患者的共同努力下,稳步走向更光明的未来。