
导语:术后PSA悄悄爬过0.2,放疗却找不到敌人藏哪儿,是扩大野还是加剂量?毒性天花板卡死,复发依旧四分之一。PSMA-PET能把微病灶拖进视野,却缺随机证据。这份研究首次把“看见就加量”写进前瞻性试验,让低PSA窗口的挽救放疗有了精准导航,或将改写术后复发的照射逻辑。
图源:CMT
术后复发灶像捉迷藏,传统影像雾里看花,PSMA-PET能否精准锁敌?RP后BCR的挽救放疗早已是“低PSA窗口”里的标准动作,但临床常被两种尴尬夹击:一是影像“看不见”导致靶区只能经验性覆盖前列腺床±全盆腔,结果25-40%患者仍在野外复发;二是即便把照射范围拉到盆腔上限,剂量却因肠膀胱耐受天花板无法再加,肿瘤控制率随PSA>0.2 ng/mL呈断崖式下跌。更棘手的是,传统CT/MR对≤5 mm淋巴结转移敏感度不足20%,胆碱PET虽略好,却受炎症和良性增生干扰,阳性预测值仅60%左右,医生往往“宁滥勿缺”却仍旧漏灶。
于是当前salvage RT陷入“范围上不去、剂量加不了、病灶找不到”的三重瓶颈:范围盲目扩大带来直肠炎、骨折、淋巴水肿等不可逆毒性;剂量受限于OAR物理阈值,EQD2 70 Gy成了前列腺床玻璃顶;而最关键的——靶区勾画依据的仍是百年解剖分区,不是肿瘤生物学实体。学界亟需一种能在低PSA阶段精准定位微小病灶、并允许“看见才加量”的影像生物标记,否则再多的调强技术都只是把“盲射”做得更精致。

2025年10月JAMA Oncology刊出的这篇PSMAiSRT研究正是把18F-DCFPyL PSMA-PET搬进随机框架,试图回答:当PET把转移灶检出率提高到骨30%、淋巴结50%以上时,放疗医生能否借助“生物可视”突破上述三重天花板,实现“同毒更高效”的靶区雕刻——而非继续困在“经验野+耐受剂量”的原始循环。
把PET阳性灶写进处方,研究者怎样在真实世界框架里做随机?本研究是一项两中心、注册嵌套、开放标签的Ⅱ期随机对照试验,旨在验证PSMA-PET引导下的挽救性放疗(PSMAiSRT)能否比标准放疗(SOC-SRT)改善失败无生存(FFS)。2018年5月至2021年2月,研究者从PSMAgRT主注册库中筛出130例RP后BCR(PSA≥0.1 ng/mL)、ECOG≤1、Charlson<5且未行12个月内ADT的患者,1:1随机,实验组先做18F-DCFPyL PSMA-PET/CT,再按病灶“加量加野”:盆腔淋巴结、前列腺床或骨转移灶分别给予EQD2(α/β1.4) 66 Gy、77 Gy或66 Gy的追加剂量;对照组按传统CT计划放疗,是否照盆腔及是否联用ADT由主管医生定。主要终点为FFS(PSA最低值≥0.2 ng/mL、影像学进展、启动下一线治疗或死亡),次要终点包括生化无复发生存、无转移生存、下次治疗-free生存、睾酮恢复后FFS及毒性/生活质量。随访截止2023年10月,中位随访37个月,意向治疗分析。
PET让靶区放大却毒性不增,FFS曲线三年拉开15%,高PSA亚组获益更抢眼三年失败率降半,图1主曲线作证
意向治疗分析显示,PSMAiSRT组仅10例出现FFS事件,对照组达20例;Kaplan-Meier估计三年失败率分别为16%与31%,HR0.46(95%CI:0.22-0.99,P=0.04,图1)。作者指出,这是首次在前瞻随机框架中证实“PET-可见即加量”能把根治术后低PSA复发者的整体进展风险砍半,而无需扩大照射野或延长ADT。
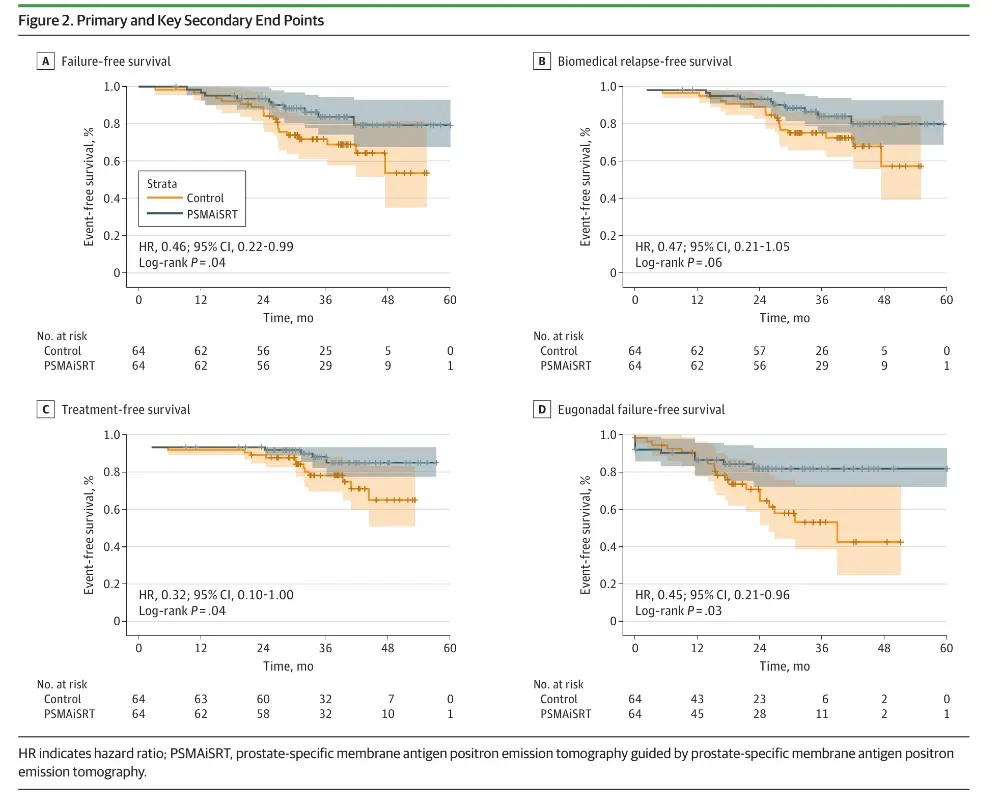
图1 主要及关键次要终点
注;HR表示风险比;PSMAiSRT表示前列腺特异性膜抗原正电子发射断层扫描引导的挽救性放疗强化。
PSA≥0.3 ng/mL亚组获益放大,图2森林图左支
预设探索性分析按入组PSA中位0.3 ng/mL切层:高值层(n=55)HR仅0.17(0.04-0.79,P=0.01),失败率绝对差异达25%;而在PSA<0.3 ng/mL层HR0.88(P=0.83)。作者解释,低负荷时PET阳性率下降,可“加量”病灶减少,稀释了效益;提示临床若PSA已≥0.3 ng/mL,应毫不犹豫先行PSMA-PET再画靶区。
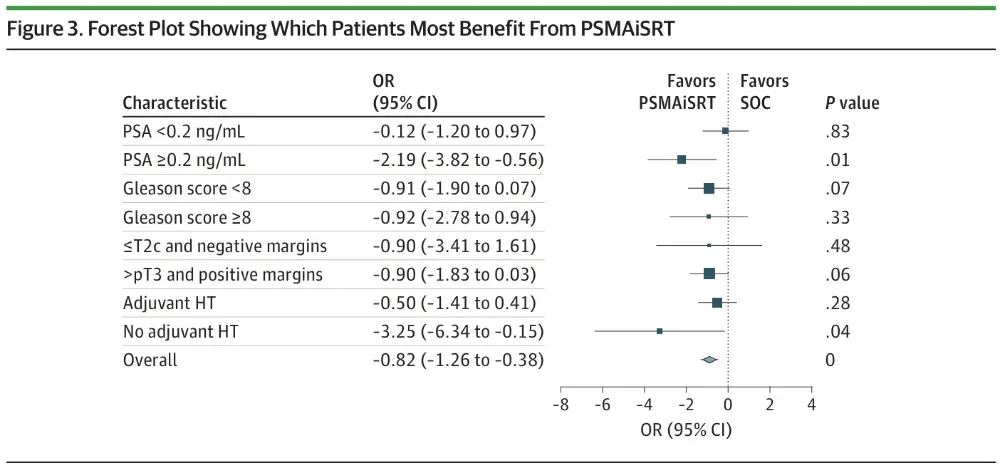
图2 哪些患者最能从PSMAiSRT中获益的森林图
注:森林图显示治疗与无失败生存之间的关系。PSMAiSRT表示前列腺特异性膜抗原正电子发射断层扫描引导的挽救性放疗强化。前列腺特异性抗原单位换算:ng/mL→μg/L乘以1。
下次治疗启动减少三分之二,图1C给出TFS
对照组12例因PSA持续升高或新转移接受二线激素或转移灶放疗,实验组仅4例;三年治疗-自由率88% vs 70%,HR0.32(0.10-1.00,P=0.04,图1C)。作者强调,这一“延迟全身治疗”的临床收益直接转化为患者更长的无药间歇与生活质量,并可能降低长期内分泌相关骨丢失与心血管事件。
恢复睾酮后依旧稳,图1D示eugonadal FFS
在意向治疗人群中,86例(67%)完成短期ADT并恢复至睾酮≥5.2 ng/dL;从达到正常睾酮算起,实验组中位失败时间尚未达到,对照组为22.3个月,HR 0.45(0.21-0.96,P=0.03,图2D)。作者认为,强化放疗清除潜在微转移,可减少睾酮回升后早期PSA反弹,对希望保留性功能的间歇ADT策略尤其重要。
生化复发有下降趋势但未跨越α,图1B列BPFS
若仅统计PSA≥0.2 ng/mL的生化事件,对照组18例,实验组9例;三年生化失败率27%vs14%,HR0.47(0.21-1.05,P=0.06,图1B)。作者坦承样本量与随访期限制了显著性,但曲线分离时间出现在放疗结束后12个月左右,符合微转移灶被追加剂量“灭菌”所需的生物学延迟,预期随Ⅲ期试验延长随访可能转正。
远处转移与总生存尚早,事件寥寥
依方案仅记录常规影像证实的远处转移,对照组4例,实验组5例;死亡各1例,均与前列腺癌无关。作者提醒,RP后低PSA队列的转移与死亡事件天然稀少,需更长时间才能看到生存差异,现阶段可把FFS与TFS作为合理替代终点。
毒性未升,生活质量未降,图3-5详列
≥2级急性胃肠-泌尿毒性两组分别为59vs60例次;≥3级事件实验组6例,对照组3例,仅1例尿道狭窄被认为与前列腺床加量至EQD2 76 Gy相关。EPIC-CP与FACT-P年度评分未出现≥2分的临床意义差异。作者总结为“isotoxic intensification”——影像引导的靶区雕刻在提高生物有效剂量的同时,仍把OAR受量锁在可接受范围。
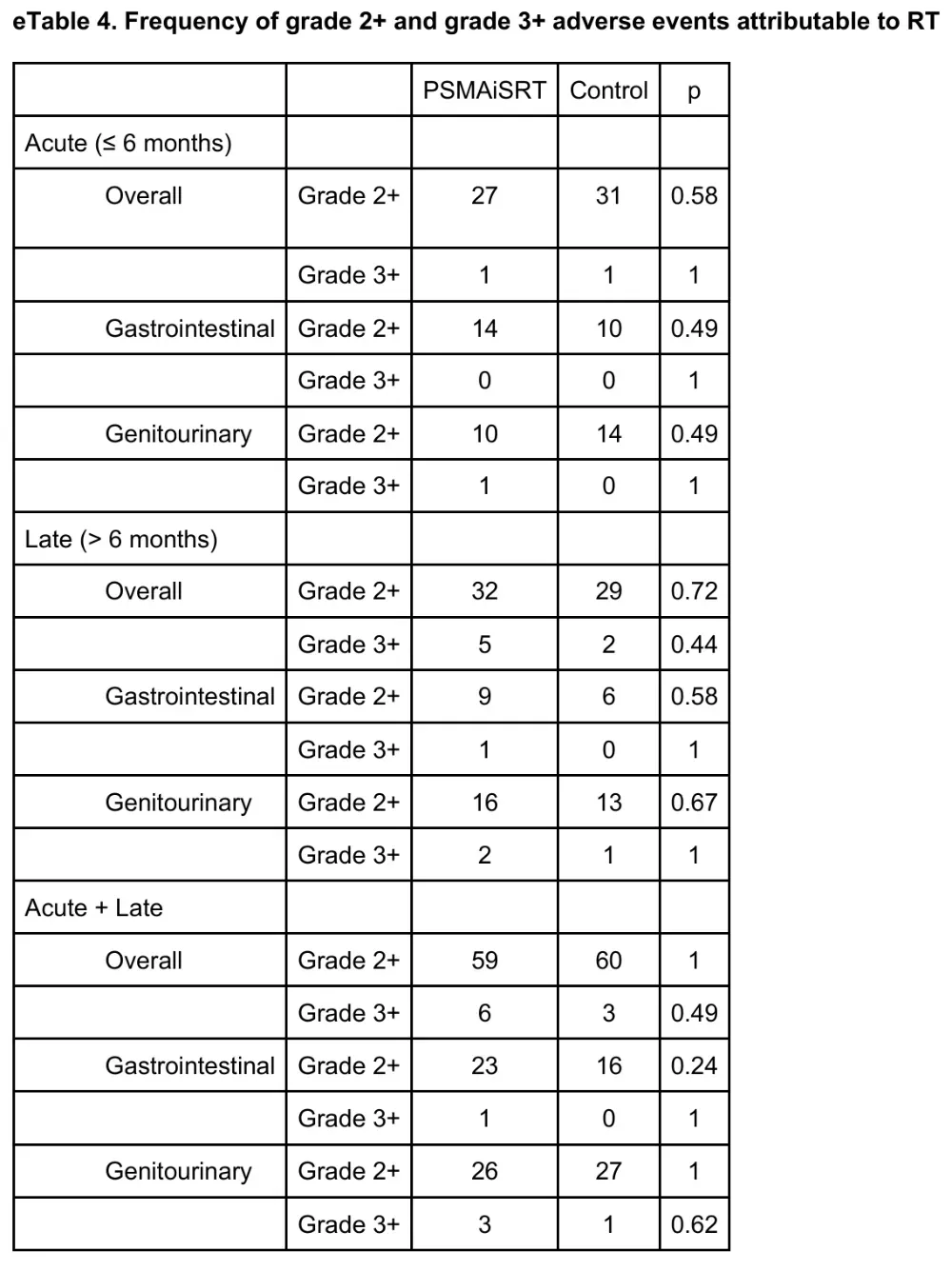
图3 归因于放疗的2级及以上和3级及以上不良事件发生率
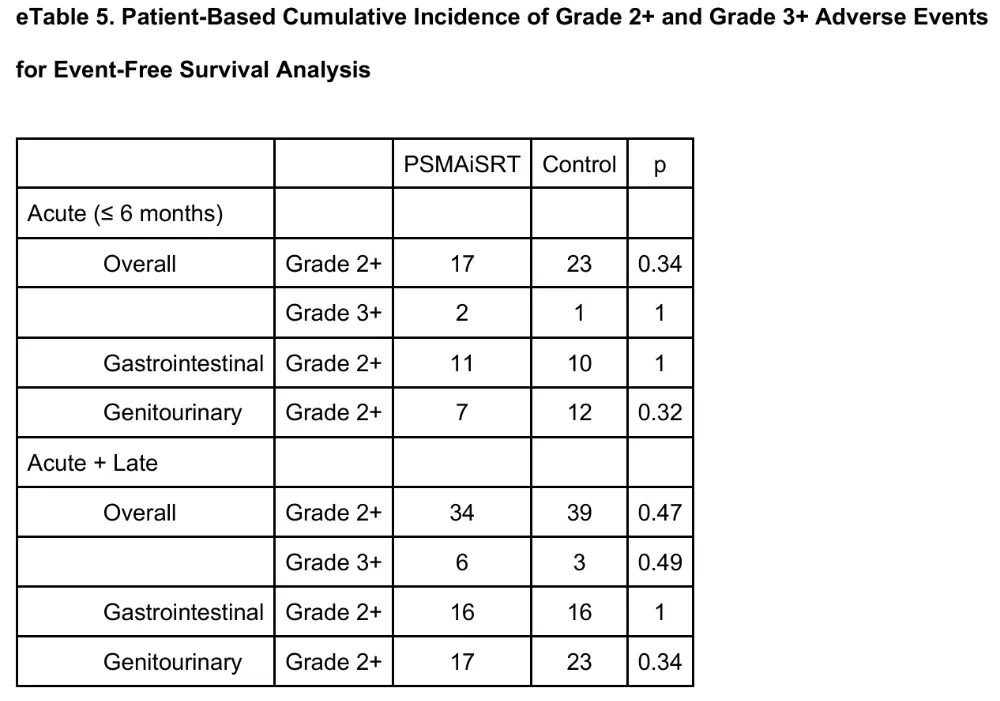
图4 用于事件无生存分析的2级及以上和3级及以上不良事件基于患者的累积发生率
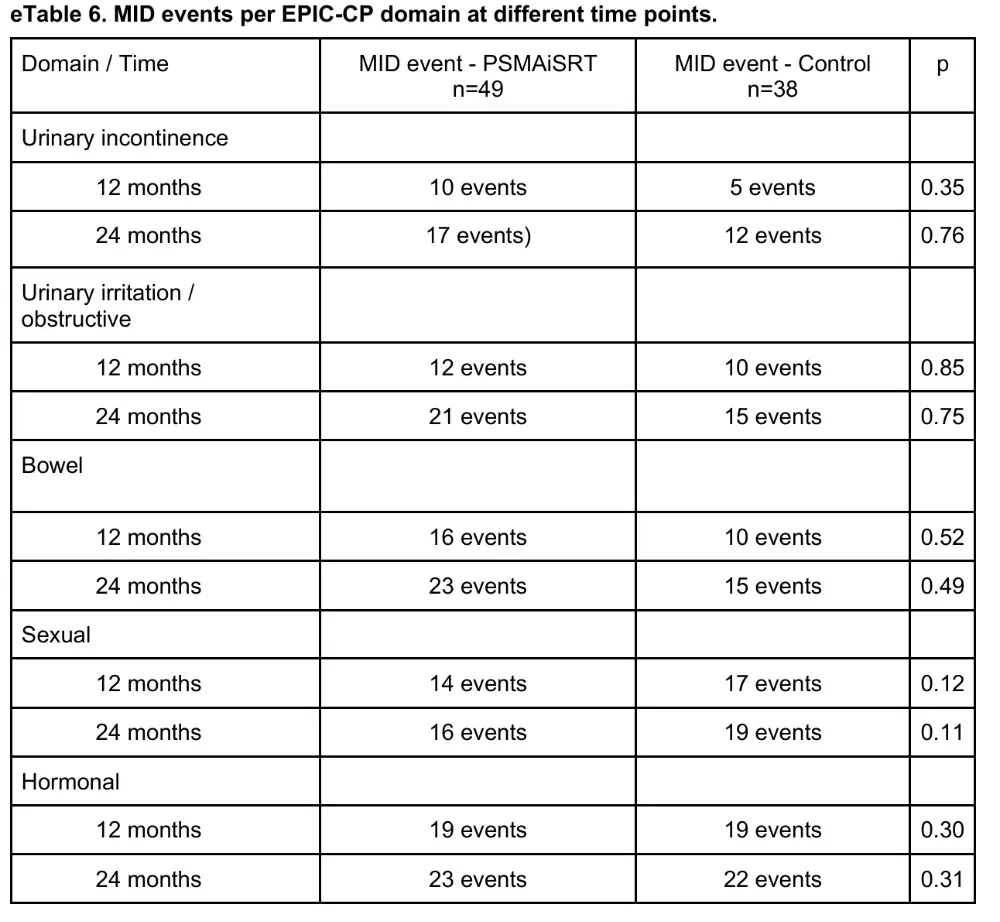
图5 不同时间点各EPIC-CP域的最小临床重要差异(MID)事件
阳性versus阴性PET患者结局相似,支持“加量即治愈”
实验组内部33例PET阳性接受强化,31例阴性按标准野治疗,后续各5例复发(15%vs16%)。作者据此推测,PET阳性病灶在EQD2 66-77 Gy范围内被有效清除,转阴后自然病史与原本阴性者一致;这也反证不加量时这些病灶极可能成为野外失败源头。
总结这项Ⅱ期随机试验首次证明,在生化复发早期把PSMA-PET嵌入挽救放疗决策,可把传统“盲照”升级为“可见即治”,三年内让失败风险降半且不必付毒性代价;尤其PSA≥0.3 ng/mL人群获益突出,为临床把握影像时机提供量化切点。尽管随访尚短、样本有限,其“isotoxic efficacy”理念为正在进行的Ⅲ期确证试验(NCT04557501)奠定理论与操作框架,也提示术后低PSA窗口期应重新评估PET导航的性价比与医保策略。
参考文献
Belliveau C, Saad F, Duplan D, et al. Prostate-Specific Membrane Antigen PET-Guided Intensification of Salvage Radiotherapy After Radical Prostatectomy: A Phase 2 Randomized Clinical Trial. [J/OL]JAMA Oncol. Published online October 2, 2025. doi:10.1001/jamaoncol.2025.3746
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:一诺
审核:白术
封面图源:CMT