在加利福尼亚州斯坦福大学的实验室里,一群神经元正在玻璃器皿中上演着人类生命最精妙的交响乐。这些来自不同脑区的细胞经过精准组装,首次在体外重现了疼痛信号从指尖传递至大脑的完整神经通路。这项发表于《自然》杂志的突破性研究,不仅揭示了人类感知系统的精密运作机制,更开辟了治疗疼痛障碍的新纪元。

一、神经通路的体外复现:从科幻到现实
斯坦福大学医学院的科研团队采用类器官培养技术,将人体背根神经节、脊髓背角、丘脑和体感皮层四个关键神经节点进行模块化组装。这种被称作"assembloid"的复合模型,成功模拟了疼痛信号在神经系统中逐级放大的完整过程。当研究人员用微电极刺激模型中的外周神经元时,电活动波以每秒15米的速度穿越各个组件,在体感皮层形成与真实人体相似的响应模式。
这项技术突破的关键在于解决了神经接口的衔接难题。项目负责人Sergiu Pasca教授指出:"不同神经组织间的信号转换就像不同语言的对话,我们开发了特殊的生物黏合剂,让来自皮肤的感觉信息能够顺畅穿越脊髓-丘脑屏障。"通过CRISPR基因编辑技术对神经元进行荧光标记,研究团队首次观测到疼痛信号在体外模型中的实时传导路径。
二、疼痛研究的范式革命
传统疼痛研究面临诸多困境:啮齿类动物模型与人类神经系统的显著差异,使得80%的镇痛药物在临床试验中宣告失败。斯坦福团队构建的体外神经高速公路,完美复现了人类特有的疼痛调制机制。当研究人员向模型中加入炎症因子模拟组织损伤时,脊髓背角的兴奋性神经元出现特征性放电模式,这种放电频率与临床慢性疼痛患者的脑电波高度相似。
更令人振奋的是,该模型具备前所未有的可控性。通过光遗传学技术激活特定神经亚型,科学家能够精确调控疼痛信号的传递强度。在最新实验中,靶向抑制丘脑中表达Nav1.7钠离子通道的神经元,成功使疼痛信号衰减率达65%,这为开发新型镇痛药物提供了关键靶点。博士后学者Ji-il Kim表示:"我们就像在神经高速公路上设置红绿灯,可以精确调控疼痛信息的流量。"
三、解锁疼痛奥秘的钥匙
这个体外神经系统的构建,为解析疼痛的神经编码提供了绝佳平台。研究团队发现,来自皮肤的伤害性信号在传递过程中会发生两次关键转化:脊髓背角神经元通过突触可塑性将短暂刺激转化为持久电活动,而丘脑则像信息过滤器一样,根据情绪和注意状态对疼痛信号进行二次调制。这种多层次的信号处理机制,揭示了为什么同样程度的物理损伤会产生截然不同的主观疼痛体验。
在药物开发领域,该模型已展现出巨大潜力。制药公司辉瑞的神经科学部门负责人表示:"我们正在利用这个系统筛选G蛋白偶联受体激动剂,初步测试显示某些化合物能够将神经元的过度兴奋状态恢复正常。"更长远来看,结合患者诱导多能干细胞技术,未来有望实现个体化的疼痛治疗。
斯坦福团队的这项研究,犹如在神经科学的迷雾中点亮了一盏明灯。当体外培养的神经元网络与人工智能算法相结合时,我们或许能真正破译大脑处理疼痛信息的"密码本"。这不仅是技术上的突破,更是人类对抗慢性疼痛这场无声流行病的里程碑式进展。正如论文通讯作者Pasca所言:"疼痛不是简单的生理反应,而是大脑编织的故事,现在我们可以开始改写这个故事的结局。"
埃泽思生物公司
埃泽思生物( Applied Cell)总部位于上海,专注于细胞治疗、再生医学等相关领域上游产品的研发与生产,公司产品在细胞与基因治疗、细胞样本存储,药物发现,科学研究等领域有广泛应用。


AC-1001042(PRF) 人脂肪干细胞无血清培养基(无酚红)

人脂肪干细胞无血清培养基是埃泽思生物(Applied Cell)自主研发的一款无外源动物成分的人脂肪干细胞培养基。可应用于人脂肪组织来源的人脂肪干细胞的扩增与传代培养,并保持其多向分化潜能。

产品特性
无外源动物蛋白成分,大大降低各类病毒、霉菌和支原体等的污染风险。
全程无血清生产,极大降低批次间差异。
培养过程无需包被培养板。
扩增效率高,24h 左右增殖翻倍,节省培养时间。
内毒素<0.06EU/ml,远低于中国药典水平。
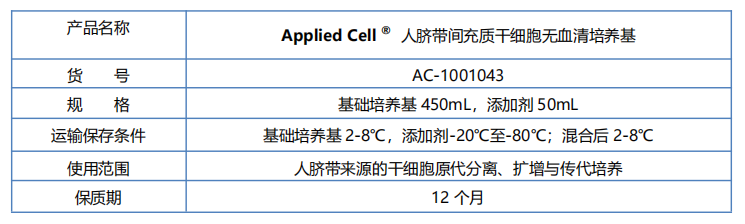
AC-1001043 人脐带间充质干细胞无血清培养基

人脐带间充质干细胞无血清培养基是埃泽思生物(Applied Cell®)自主研发的一款无外源动物成分的人间充质干细胞培养基。可应用于人脐带组织来源的干细胞的原代分离、扩增与传代培养,并保持其多向分化潜能。本产品内毒素水平远低于中国药典标准,生产过程遵循 ISO9001 体系,并符合 GMP 指导原则。
产品特性
无外源动物蛋白成分,大大降低各类病毒、霉菌和支原体等的污染风险。
全程无血清生产,极大降低批次间差异。
可用于原代分离,且培养过程无需包被培养板。
扩增效率高,24h 左右增殖翻倍,节省培养时间。
内毒素<0.06EU/ml,远低于中国药典水平